正大天晴、科伦、康缘...15个重磅首仿将获批
凭借着市场和定价优势,首仿药一直以来都是国内药企研发布局的重点。新年伊始,已有多款首仿药(含剂型首仿)获批上市,包括扬子江的瑞戈非尼片、苏州特瑞药业的尼洛替尼胶囊、浙江尔婴药品的艾司奥美拉唑镁肠溶干混悬剂等。那么还有哪些重磅首仿药有望于2023年底前获批上市呢?
2023年有望获批的重磅首仿药
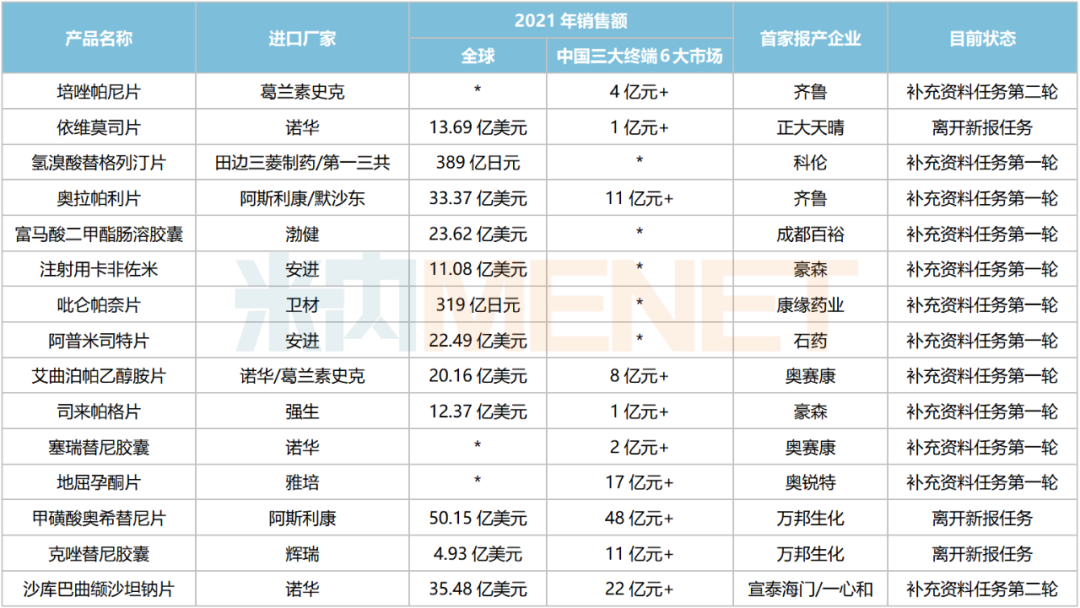
注:无销售额或销售额较低用*代表;预测数据,仅供参考;首家报产不一定首家获批
来源:米内网综合数据库
全球首款治疗心衰创新药,超10家药企争抢
沙库巴曲缬沙坦是由沙库巴曲(脑啡肽酶抑制剂)和缬沙坦(血管紧张素受体拮抗剂)组成的复方制剂,于2015年7月获得FDA批准上市,是全球首款心衰治疗领域的突破性创新药物,原研产品2021年全球销售额达35.48亿美元。
近年来中国三大终端6大市场沙库巴曲缬沙坦钠片销售情况(单位:万元)
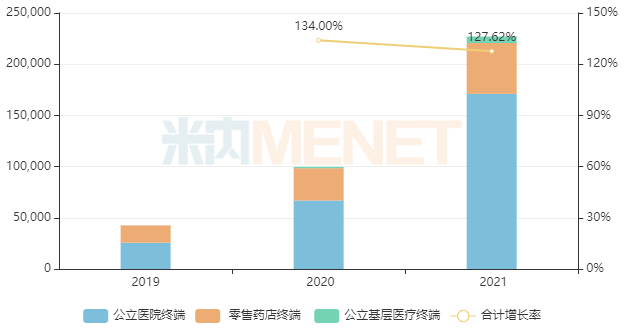
来源:米内网格局数据库
2017年7月,诺华的沙库巴曲缬沙坦钠片首次获批进入国内市场,2019年通过谈判纳入全国医保乙类目录,2021年成功续签,并新增原发性高血压适应症。米内网数据显示,该产品近年来在中国三大终端6大市场(统计范围详见本文末)的销售额增速均达三位数,2021年首次突破20亿元,同比增长127.62%,市场潜力十足。
沙库巴曲缬沙坦钠片新分类报产情况
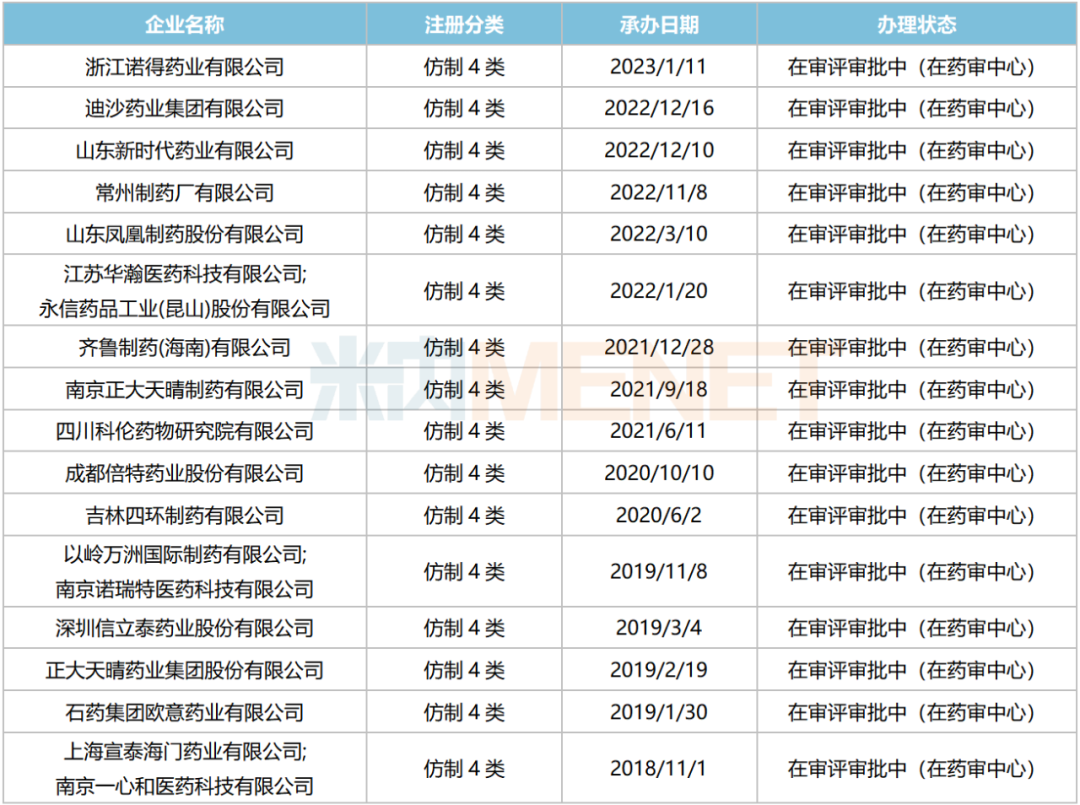
来源:米内网中国申报进度(MED)数据库
目前国内有超10家企业以仿制4类提交沙库巴曲缬沙坦钠片上市申请,其中上海宣泰海门/一心和最早报产,其上市申请于2018年11月获得CDE承办受理,目前正处于第二轮资料发补。此外,石药欧意、正大天晴、信立泰等企业的产品处于第一轮资料发补。
多家药企屡受挫的高难度品种,谁将最终突围?
阿普米司特片(曾用名:阿普斯特片)是由新基研发的一种磷酸二酯酶-4(PDE-4)抑制剂(后被安进购入),最早于2014年获得FDA批准上市,为过去二十多年首个治疗银屑病/银屑病关节炎的口服新药,2021年全球销售额达22.49亿美元。
阿普米司特片新分类报产情况
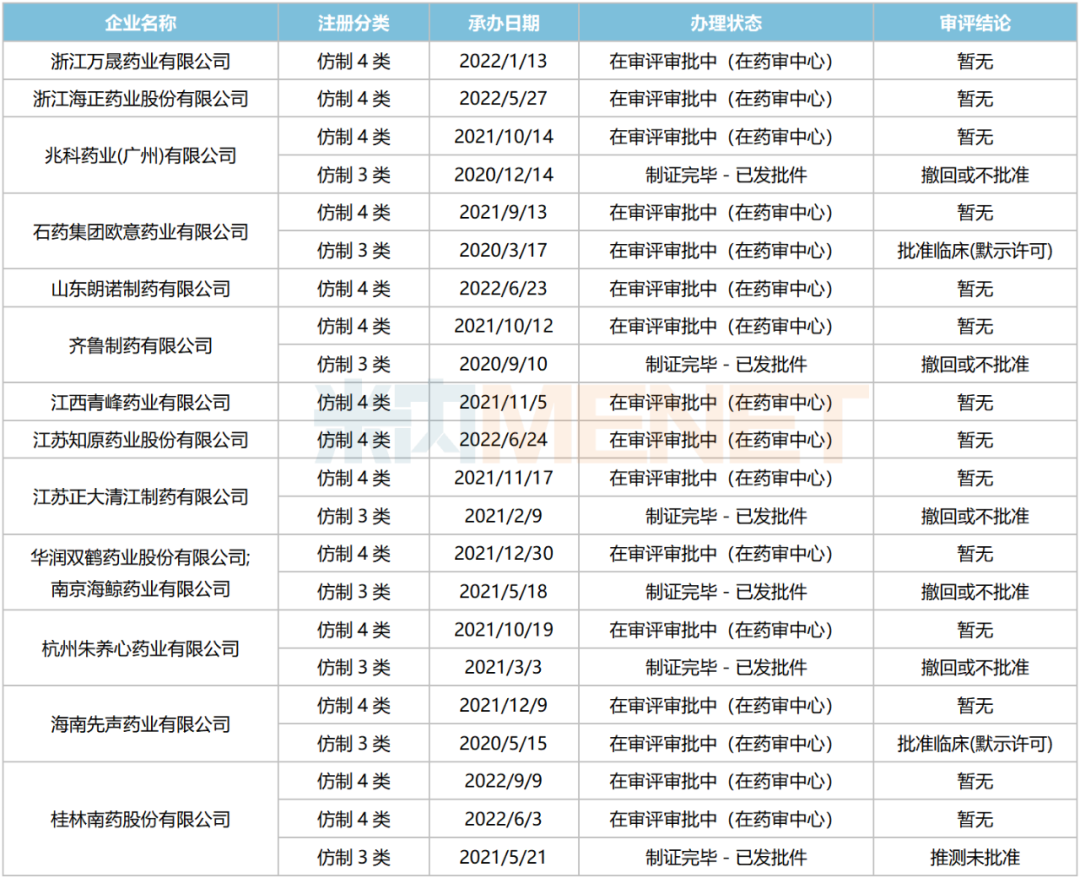
来源:米内网中国申报进度(MED)数据库
原研产品于2021年8月获批进入国内市场,目前有超10家国内药企以新注册分类提交阿普米司特片上市申请,但多家药企的产品在首次申报时折戟成沙,终未获批。
从目前申报进度看,阿普米司特片首仿之争战况胶着,石药欧意的产品虽为首家,但齐鲁、兆科药业、杭州朱养心药业等企业也纷纷进入第一轮补充资料,谁将突围而出?我们拭目以待。
48亿大品种,江苏万邦生化率先进攻
奥希替尼为阿斯利康研发的第三代口服、不可逆的选择性EGFR突变抑制剂,是全球第一个上市,也是中国首个获批的用于EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌的肿瘤药物,2021年全球销售额达50.15亿美元。
近年来中国三大终端6大市场甲磺酸奥希替尼片销售情况(单位:万元)
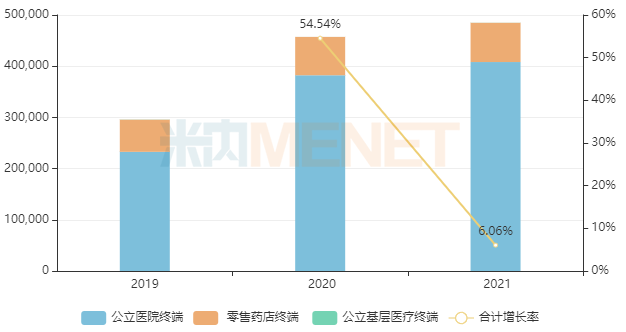
来源:米内网格局数据库
2017年3月,阿斯利康的甲磺酸奥希替尼片首次获批进入国内市场,2018年通过谈判纳入全国医保乙类目录,2020年成功续签,一线及二线适应症全部纳入,有望实现进一步放量。米内网数据显示,该产品2021年中国三大终端6大市场的销售额超过48亿元,同比增长6.06%。
甲磺酸奥希替尼片研发进度
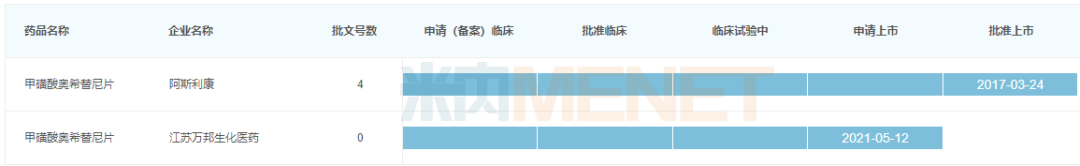
来源:米内网中国申报进度(MED)数据库
奥希替尼国内化合物专利CN103702990将于2032年7月到期,目前仅江苏万邦生化布局仿制药,其产品于2020年8月完成BE试验,并于2021年5月以仿制4类递交上市申请,目前已离开新报任务。
罕见病用药,豪森药业首家报产
司来帕格是由强生开发的口服IP前列环素受体激动剂,可改善损伤的肺动脉内皮依赖性舒张,并可能抑制人肺平滑肌细胞的增殖、肺血管壁的增厚,是一款罕见病用药,2021年全球销售额达12.37亿美元。
原研产品于2018年12月获批进入国内市场,目前已通过谈判纳入全国医保乙类目录,该产品2021年在中国三大终端6大市场的销售额超过1亿元,同比增长263.1%,市场潜力在逐步释放。
司来帕格片新分类报产情况
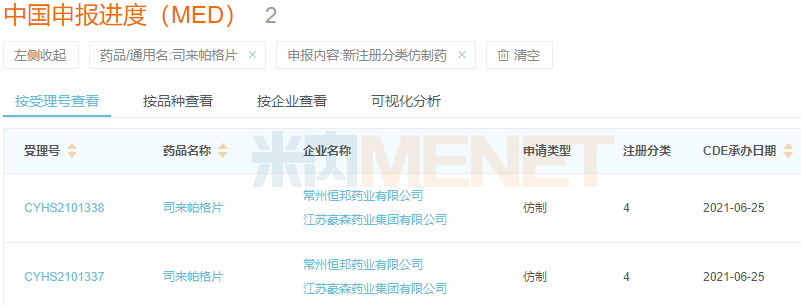
来源:米内网中国申报进度(MED)数据库
豪森药业的司来帕格片于2021年3月完成BE试验,并于2021年5月以仿制4类递交上市申请,目前处于处于第一轮资料发补。
全球首个mTOR抑制剂,正大天晴有望突围
依维莫司是由诺华研发的一款哺乳动物雷帕霉素靶蛋白(mTOR)抑制剂,于2009年在美国获批上市,是FDA批准的首个mTOR抑制剂,2021年全球销售额为13.69亿美元。
原研产品于2013年1月获批进入国内市场,2017年通过谈判纳入全国医保乙类目录,目前已有5个适应症被纳入其中。米内网数据显示,该产品2021年在中国三大终端6大市场合计销售额超过1亿元,呈稳中带升态势。
依维莫司片新分类报产情况

来源:米内网中国申报进度(MED)数据库
正大天晴药业最早于2018年11月提交依维莫司片上市申请,未被批准,公司于2022年1月再次报产,目前已离开新报任务。
全球首个PARP抑制剂,齐鲁首家报产
奥拉帕利属于PARP抑制剂,通过抑制PARP,减少甚至阻止携带有受损BRCA基因的癌细胞进行DNA修复,达到杀死癌细胞死亡的目的。该产品由阿斯利康/默沙东联合研发,最早于2014年12月获得FDA批准上市,为全球首款PARP抑制剂,2021年全球销售额达33.37亿美元。
近年来中国三大终端6大市场奥拉帕利片销售情况(单位:万元)
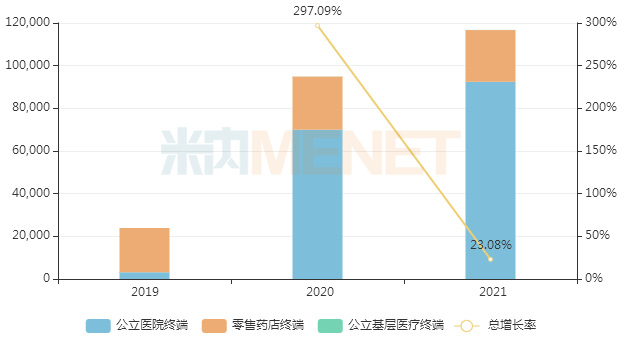
来源:米内网格局数据库
2018年8月,阿斯利康的奥拉帕利片首次获批进入国内市场,2019年通过谈判纳入全国医保乙类目录,2020年成功续签并新增适应症。米内网数据显示,近年来奥拉帕利片在中国三大终端6大市场的销售规模逐年上涨,2021年首次突破10亿元,同比增长23.08%。
奥拉帕利片新分类报产情况

来源:米内网中国申报进度(MED)数据库
目前国内有6家药企以新注册分类提交奥拉帕利片上市申请,其中齐鲁制药首家报产,目前处于第一轮资料发补。
全球首个ITP口服药,4家药企最后角逐
艾曲泊帕乙醇胺是诺华/葛兰素史克开发的一种非肽类血小板生成素受体(TPO-R)激动剂,于2008年11月获得FDA批准上市,为全球首个治疗原发免疫性血小板减少症(ITP)的口服药物,2021年全球销售额达20.16亿美元。
近年来中国三大终端6大市场艾曲泊帕乙醇胺片销售情况(单位:万元)
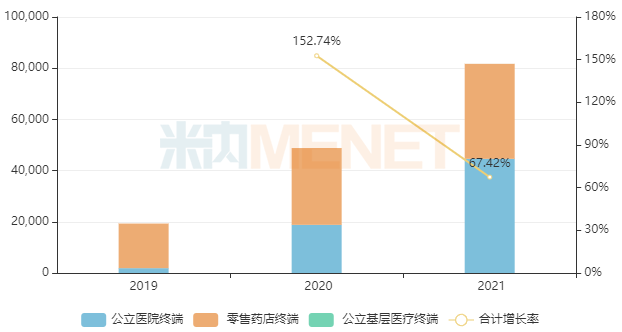
来源:米内网格局数据库
原研产品于2017年12月获批进入中国市场,目前已通过谈判纳入全国医保乙类目录。随着适应人群的拓展,艾曲泊帕乙醇胺片在国内市场快速放量,该产品2021年中国三大终端6大市场的销售额突破8亿元,同比增长67.4%。
艾曲泊帕乙醇胺片新分类报产情况

来源:米内网中国申报进度(MED)数据库
多家国内药企布局艾曲泊帕乙醇胺仿制药,其中奥赛康的产品首家报产,但正大天晴、齐鲁、科伦3家企业也已进入第一轮补充资料,首仿或将在这4家企业之中诞生。
资料来源:米内网数据库等
【版权声明】秉承互联网开放、包容的精神,医药网欢迎各方(自)媒体、机构转载、引用我们原创内容,但要严格注明来源医药网;同时,我们倡导尊重与保护知识产权,如发现本站文章存在版权问题,烦请将版权疑问、授权证明、版权证明、联系方式等,发邮件至pharmnet@netsun.com,我们将第一时间核实、处理。
- 相关报道
-
- 仿制药获批TOP20企业!扬子江领跑,科伦、恒瑞7个首仿霸屏(2023-02-01)
- 15个重磅首仿药有望获批 角逐超100亿市场(2023-01-29)
- 倍特药业拿下18个重磅首仿 20个品种首家过评(2022-12-26)
- 11月6个1类中药新药申报,7个首仿品种获批(2022-12-06)
- 豪森拿下13个首仿、6款新药,29款1类新药来势汹汹(2022-11-24)
- 19个超$10亿品种首仿在路上 正大天晴等出击(2022-10-21)
- 奥赛康火力全开!拿下4个重磅首仿、20个过评品种(2022-09-30)
- 恒瑞、禾亿拿下眼科用药首仿,7个独家过评品种亮眼!(2022-08-30)
- 造影剂TOP10排位生变 恒瑞、科伦拿下首仿(2022-08-19)
- 豪森31款新药、6个首仿冲刺,41个品种过评(2022-07-28)



